|
|
|
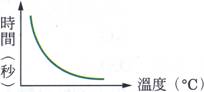
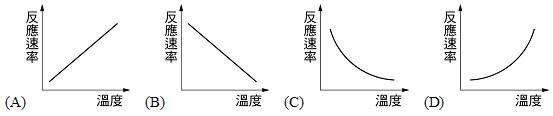
(一)溫度和反應速率 A、 溫度的高低和【反應速率】有很大的關係。 B、 依【碰撞】學說: C、 溫度對反應速率最直接的影響為: D、 在實驗室中,欲增加反應速率,最有效的方法為【加熱】。 E、 生物體內的化學反應都需要酵素 (生物體內的催化劑,蛋白質為主要成分) 參與反應,由於溫度太高會破壞蛋白質成分,因此生物體的溫度不能太高。 F、 溫度愈高,反應速率愈快,但【不成正比】。
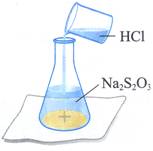
(二)硫代硫酸鈉和鹽酸反應 A、 B、 實驗步驟: (1)
瓶底對準十字符號放置。 (2)
加入硫代硫酸鈉(Na2S2O3)及鹽酸(HCl)溶液,並開始計時。 (3)
當黃色的硫沉澱產生至一定量時,會遮住白紙上的十字,測量開始反應至遮住十字的時間。 (4)
每次實驗固定溶液的濃度,測量不同溫度下的反應速率,如此重複實驗。 C、 討論: (1)
此實驗在探討【溫度】和反應速率的關係。 (2)
此實驗在觀察反應後【黃色】硫沉澱的快慢。 (3)
每次反應,改變溫度,但是每次的沉澱量皆相等(遮住十字的沉澱量和溫度無關)。 |
|
一、選擇題: ( )1.
最容易使穩定化合物發生化學變化的方法是 【解答】:【D】 【解析】: ( )2.
溫度升高時,一般化學反應之速率均有顯著增加,其主要原因為何? 【解答】:【B】 【解析】: ( )3.
燃燒蠟燭時『用火點燃』的目的是 【解答】:【D】 【解析】: ( )4.
為何點燃蠟燭時需用火柴? 【解答】:【C】 【解析】: ( )5.
煤氣和空氣的混合物,點火就立刻劇烈地反應,歸因下列何種影響反應速率的因子?(A)催化劑 (B)顆粒大小 (C)溫度 (D)濃度。 【解答】:【C】 【解析】: ( )6.
硫代硫酸鈉溶液中,加入鹽酸而加熱,生成暗黃色固體沈澱物是 【解答】:【B】 【解析】: ( )7.
研究硫代硫酸鈉和鹽酸反應的速率,觀察下列何項,較為方便? 【解答】:【C】 【解析】: ( )8.
何組溶液混合時不產生白色沈澱? 【解答】:【D】 【解析】: ( )9.
能使硫代硫酸鈉溶液與鹽酸加速反應的方法有那些? 【解答】:【C】 【解析】: ( )10.
將 【解答】:【D】 【解析】: ( )11.
溫度升高對於反應速率具有那些效應? 【解答】:【D】 【解析】: ( )12.
下列圖形為Na2S2O3 +
2HClè2NaCl + H2O + SO2 +
S 之反應速率實驗,假設H+濃度一定,S2O32- 的濃度分別為0.lM、0..2M、 【解答】:【D】 【解析】: ( )13.
在常溫下除反應自發熱能外,皆不另外加熱時,下列反應速率何者最小? 【解答】:【A】 【解析】: ( )14.
化學實驗室中,欲使反應發生,常用酒精燈或本生燈加熱,是因 【解答】:【D】 【解析】: ( )15.
我們知道汽油可燃燒,但將其曝露於空氣中,不經點燃,不發生燃燒,是因為 【解答】:【D】 【解析】: ( )16.
某生夜晚返家時,家中空無一人,亦未開電燈,但此時家中因煤氣開關未旋緊而使室內充滿煤氣,則該生應採取何種安全有效的措施? 【解答】:【B】 【解析】: ( )17.
下列有關硫代硫酸鈉溶液和鹽酸發生反應的敘述,何者是正確的? 【解答】:【B】 【解析】:溫度愈高,分子具有的能量愈大,產生的反應速率會愈快,發生的時間會愈短。 ( )18.
下列何者正確? 【解答】:【C】 【解析】:(A) 硫代硫酸鈉和鹽酸作用,所生黃色沈澱是硫,是元素,不是化合物。 ( )19.
取同為 【解答】:【A】 【解析】: ( )20.
沒塞橡皮塞的甲、乙兩試管,各裝 【解答】:【B】 【解析】: ( )21.
若取同為 【解答】:【A】 【解析】: ( )22.
CaCO3+2HCl → CaCl2+H2O+CO2反應中,加水會使二氧化碳生成速率有何變化? 【解答】:【B】 【解析】:加水使濃度減少,因此反應速率減慢。 ( )23.
下列關於反應速率之說明,何者正確? 【解答】:【B】 【解析】: ( )24.
在Na2S2O3+2 HCl→SO2+2 NaCl+H2O+S之反應速率實驗中,若鹽酸水溶液濃度一定,硫代硫酸鈉水溶液濃度各為 【解答】:【B】 【解析】: ( )25.
【解答】:【C】 【解析】: ( )26.
將 Na2S2O3溶液與HCl溶液放入錐形瓶中,觀察沉澱將瓶下所畫的圖案遮住,並測量所需的時間t,下列何者可代表該反應的反應速率? 【解答】:【B】 【解析】: ( )27.
在Na2S2O3+2HCl→2NaCl+SO2+H2O+S反應中,若欲觀察反應的速率,則應觀察下列哪一項會比較明顯而容易? 【解答】:【D】 【解析】: ( )28.
小語的鮮奶沒喝完,卻忘記放入冰箱中冷藏,隔夜鮮奶就壞掉了,這是哪一個反應速率的變因所造成的結果? 【解答】:【A】 【解析】: ( )29.
汽油可以燃燒,但將其曝露於空氣中,不經點燃,常不發生燃燒,這是因為: 【解答】:【D】 【解析】: ( )30.
為什麼加熱有助於麵糰發酵? 【解答】:【D】 【解析】:
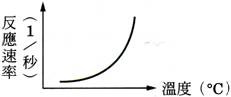
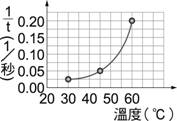
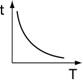
【解答】:【C】 【解析】:(C)橫坐標愈大,縱座標也愈大,溫度愈高,則反應速率愈快,一般將時間的倒數視為反應速率,所以縱座標為時間倒數。 ( )32.
【解答】:【C】 【解析】: ( )33.
做化學實驗時,通常以酒精加熱,其用意是: 【解答】:【B】 【解析】: ( )34.
取 【解答】:【A】 【解析】: ( )35.
定量的食鹽溶於水中,下列哪一種操作方法可以增加溶解速率,且不會影響溶解度? 【解答】:【C】 【解析】: ( )36.
假設溫度每升高 【解答】:【C】 【解析】:192( ( )37.
就平衡「A+B→C+D+熱量」而論,下列四種方法中,何者為增加D產量最適宜的方法? 【解答】:【C】 【解析】:為了使D物質增加,須使反應向右進行,因此從平衡觀點,加入A物質或加入B物質,都能使反應向右邊,或是減少C物質,也可以反應向右邊。 ( )38.
取20℃, 【解答】:【C】 【解析】:20℃時需要50秒時間,反應速率R1=1/50; ( )39.
下列有關反應速率的敘率,何者錯誤? 【解答】:【C】 【解析】: ( )40.
能使硫代硫酸鈉與鹽酸溶液反應的速率加速的方法為何? 【解答】:【C】 【解析】: ( )41.
在CaCO3+2HCl→CaCl2+CO2+H2O的反應,何種處理方式可降低其反應速率? 【解答】:【D】 【解析】:(D) 加水稀釋,會導致濃度降低,減少反應速率。 ( )42.
假設溫度每升高 【解答】:【C】 【解析】:48秒( ( )43.
在Na2S2O3+2 HCl→SO2+2 NaCl+H2O+S之反應速率實驗中,若鹽酸溶液濃度一定,硫代硫酸銅溶液濃度各為 【解答】:【C】 【解析】: ( )44.
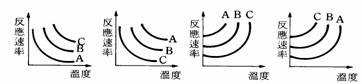
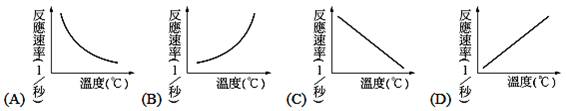
溫度對反應速率的影響,溫度與反應速率關係圖下列何者正確? 【解答】:【B】 【解析】: ( )45.
家庭中吃過的剩菜,放在冰箱中冷藏,可保存1∼2天不腐敗。但在夏天,剩菜置於桌上,很容易變質,依照反應速率而言,這是哪一種因素的影響? 【解答】:【A】 【解析】: ( )46.
在便利商店所賣的御飯團,常以 【解答】:【A】 【解析】: ( )47.
實驗室中常以下列兩種操作方式使反應加快,(甲)將藥品配成溶液,(乙)加熱。這是改變哪些因素以影響其反應速率? 【解答】:【C】 【解析】: ( )48.
有關反應速率之說明,下列何者正確? 【解答】:【B】 【解析】: ( )49.
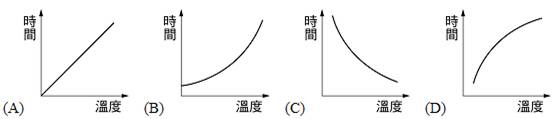
若用圖形表示硫代硫酸鈉與鹽酸反應速率受溫度的影響,則下列何者正確? 【解答】:【D】 【解析】: ( )50.
取 【解答】:【D】 【解析】: ( )51.
影響反應速率的因素有:(甲)濃度;(乙)溫度;(丙)接觸面積; 【解答】:【D】 【解析】:濃度愈大,反應速率愈快;溫度愈高,反應速率愈快,接觸的表面積愈大,反應速率愈快,因此都有關係。 ( )52.
在Na2S2O3+2HCl→2NaCl+SO2+H2O+S反應中,取3.16公克的Na2S2O3與足量的HCl作用,可得到多少公克的S?(原子量:Na=23,O=16,S=32) 【解答】:【B】 【解析】:Na2S2O3+2HCl→2NaCl+SO2+H2O+S<br/> ( )53.
下列何者是利用反應時,因為溫度的關係,使得反應速率改變的實例? 【解答】:【B】 【解析】: ( )54.
下列操作方法:(甲)將反應物顆粒研磨成粉末;(乙)降低反應時的溫度;(丙)將反應物溶液加水稀釋;(丁)將可溶性的反應物配成溶液。可使反應速率變快共有幾項? 【解答】:【B】 【解析】: ( )55.
下列有關化學反應的敘述,何者正確? 【解答】:【C】 【解析】: ( )56.
取 【解答】:【B】 【解析】: ( )57.
霽宇的爸爸去海邊釣魚,釣上來的漁貨就放入帶來的大水桶中,如果爸爸想讓霽宇吃到比較新鮮的漁貨,他該如何處理呢?(假設魚釣上來之後便立刻死亡) 【解答】:【C】 【解析】: ( )58.
下列有關化學反應的敘述,何者錯誤? 【解答】:【D】 【解析】: ( )59.
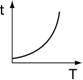
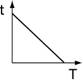
以硫代硫酸鈉與鹽酸反應,研究溫度與反應速率之關係,若以t代表反應時間,T代表溫度,則下列何者為正確圖形? 【解答】:【A】 【解析】: |
|
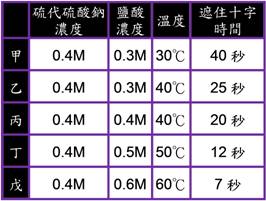
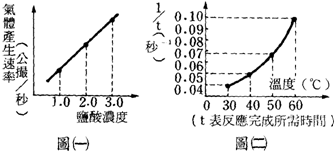
二、填充題: 1. 在錐形瓶底畫十字,做硫代硫酸鈉與鹽酸的實驗。一、二、三次中硫代硫酸鈉溶液的溫度依序為 (1) 【第三次】反應速率最快,為第二次的【5/3】倍。 (2) 當十字被遮住時,那一次的硫產量最多?【相等】。 (3) 為使硫代硫酸鈉溶液溫度達 2. (1) 欲探討濃度和反應速率的關係,應比較那幾次實驗? (2) 欲探討溫度和反應速率的關係,應比較那幾次實驗? (3) 戊的速率為丁的幾倍?【12/7】。 3. 根據下列兩個實驗結果回答下列問題: (1) 由圖(一)可知何種因素會影響化學反應速率?【濃度】。 實驗二:一定濃度的硫代硫酸鈉溶液10公撮+ (2) 由圖(二)可知何種因素曾影響化學反應速率?【溫度】。
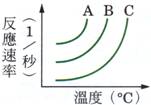
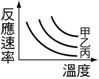
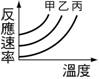
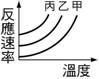
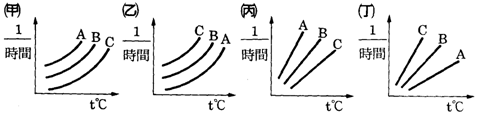
(3) 由實驗(二),在 4. 以不同濃度的A、B、C之硫代硫酸鈉與鹽酸反應結果如圖,則: (1) 相同溫度下【A】的反應時間最短。 (2) 濃度大小依次為【A>B>C】。 (3)
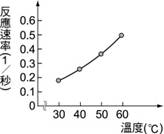
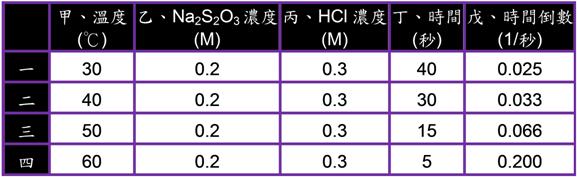
若改以時間倒數作圖則何者正確?【甲】。 5. 在畫有十字記號的白紙上置錐形瓶,瓶底中心對準十字,在錐形瓶內加入定量的Na2S2O3及HCl溶液,一邊用手輕輕搖動錐形瓶,一邊開始計時直至瓶中溶液顏色恰可遮住白紙上的十字。如表為四次實驗的記錄,圖中是將時間倒數對溫度所繪成的曲線圖,回答下列問題:
(1) 本實驗的反應式:【Na2S2O3+2HCl→2NaCl+H2O+SO2+S】; (2) 依據上表,本實驗探討那兩個量關係?【D】 (3) 實驗得知:溫度愈高,反應速率【愈快】。 (4) 若四次實驗在停止計時的瞬間,遮住十字架的產量分別為W、X、Y、Z,則四者大小順序為【相等w=X=Y=Z】。 (5) 由圖推知 (6) 下列有關本實驗的四個變因: (7) 本實驗時,主要的離子反應方程式為【S2O32-+2H+→H2O+SO2+S】。 (8) 戊欄中時間的倒數表示【反應速率】,與時間成【反比】。 (9) 第一次實驗時,取 6. 有關如下之實驗,裝有l (1) 硫代硫酸鈉與鹽酸混合後所生成的暗黃色物質為【硫S】。 (2) (3) 將沈澱過濾後的濾液加熱蒸乾,則可得何種鹽類?【氯化鈉NaCl】。 (4) 能使硫代硫酸鈉溶液與鹽酸加速反應的方法有那些?【CD】 (5) ]按照碰撞學說,欲使化學反應在短時間內完成,最好的方法是【加熱】。 (6) 家庭中的飯菜放在冰箱內 (7) 硫代硫酸鈉和鹽酸的反應會產生有刺激臭味的【二氧化硫(SO2)】氣體,並且有【黃色】的【硫】沉澱。 |