|
|
||||||||||||||||||||||||||||||
|
(一) 莫耳濃度 A、定義:平均每1公升的溶液中含有溶質的莫耳數,即稱為【莫耳濃度】。 B、公式:莫耳濃度(M)=【莫耳數】÷【公升】
溶質的莫耳數(mole)=【M】×【L】 C、單位:【M】(【mole/L】) 【說明】:溶液的配置: ◎ 配置 ◎ 配置 (二)
莫耳濃度的應用 A、稀釋(高濃度à低濃度) (1)
溶液稀釋時,溶質的莫耳數不變。 (2)
設法先求出溶質的莫耳數。( 莫耳數=【M】×【L】) (3)
新濃度=【mole(原莫耳數) ÷ L(稀釋後總體積)】。 【說明】:原溶液的莫耳數 = M1 × L1 稀釋時加水不加溶質,因此溶質的莫耳數維持不變。 B、溶液混合(相同溶質,不同濃度) (1) 先求出個別的溶質莫耳數(莫耳數=【M】×【L】) (2)
求莫耳數的總和。 (3)
求混合的總體積。 (4)
混合濃度=【mole(總莫耳數)】÷【L(混合總體積)】。 【說明】:原溶液的莫耳數 = M1 × L1+M2 × L2 混合溶液的總體積= L1+L2 混合溶液的濃度MNEW= mole/L=(M C、重量百分率濃度和莫耳濃度的換算 假設溶液體積有1公升(1000㏄),則: (1) 溶液質量M=【溶液體積1000 cc】×【溶液密度D】 (2) 溶質重=【溶液質量M】×【重量百分率濃度 %】。 (3) 溶質莫耳數=【溶質重量】÷【分子量】。 (4)
溶液的莫耳濃度=【溶質莫耳數】÷【溶液體積( 【說明】:密度 假設溶液有1000cc(1公升),則: 溶液的莫耳濃度=8莫耳/1公升= 可以用1個式子表示: 例1.(1) (2) 【解析】:M=莫耳/升=6莫耳÷
【解析】:M=莫耳/升=6莫耳÷
【解析】:M=莫耳/升=2莫耳÷
【解析】:M=莫耳/升=M÷L=M/L
例3.
《題型二》
例4. 《題型三》 若原子量 Na=23,H=1,O=16,N=14,S=32,Cu=64 ,則:
例5. 《題型四》 溶液的稀釋:
例6. 《題型五》 溶液的混合:
例7.《題型六》 重量百分率濃度和莫耳濃度的換算:
|
||||||||||||||||||||||||||||||
|
一、選擇題: ( )1.
一莫耳葡萄糖(C6H12O6),下列敘述何者正確? 【答案】:(C) 【解析】:1莫耳葡萄糖(C6H12O6)含有1莫耳的分子,共有6莫耳的C原子,12莫耳的H原子,6莫耳的O原子, ( )2.
通入3×1023個氯化氫分子於純水中,量得此溶液體積為500毫升,則氫離子濃度為若干? 【答案】:(C) 【解析】: ( )3.
蔗糖分子式為C12H22O11, 【答案】:(D) 【解析】: ( )4.
欲配 【答案】:(B) 【解析】: ( )5.
200毫升的0.5MH2SO4溶液,與300毫升、1MH2SO4溶液混和,下列敘述何者錯誤? 【答案】:(D) 【解析】: ( )6.
甲燒杯含有 【答案】:(B) 【解析】: ( )7.
有濃度 【答案】:(B) 【解析】: ( )8.
等體積的溶液含等重溶質,下列各種溶液中何者莫耳濃度最大?(Ag=108,N=14,S=32,Cu=64,Na=23,
Cl=35.5) 【答案】:(C) 【解析】: ( )9.
1毫升、 【答案】:(D) 【解析】: ( )10.
氯化鈉晶體在 【答案】:(B) 【解析】: ( )11.
甲燒杯中含 【答案】:(B) 【解析】: ( )12.
等體積的溶液中含等重的溶質,下列各種溶液中,何者的莫耳濃度最大? 【答案】:(C) 【解析】: ( )13.
1毫升、 【答案】:(D) 【解析】: ( )14.
一瓶食鹽水倒掉1/3體積後加滿水,濃度變為 【解析】: ( )15.
【答案】:(A) 【解析】: |
||||||||||||||||||||||||||||||
|
二、填充題: 1.
大雄秤36克的葡萄糖加水至800毫升,則: (1)葡萄糖的分子式為【C6H12O6】,分子量為【180】。 (2)此溶液含葡萄糖溶質【0.2】莫耳,碳原子【7.2×1023】個,共含【4.8】莫耳原子; (3)此溶液的莫耳濃度為【0.25】M; (4)再將此溶液再加水稀釋至【4】升時,濃度為 0.05 M。 【解析】:(1) C6H12O6分子量=12×6+1×12+16×6=180 2.
將2M食鹽水1升,和0.5M食鹽水2升相混合,請回答下列問題:(Na:23,Cl:35.5) (1)混合溶液中所含的溶質莫耳數共【3】莫耳。 (2)混合溶液中所含的溶質共【175.5】克。 (3)將此混合溶液取出 200 毫升,其中含溶質【11.7】克。 【解析】:(1) 總莫耳數=2×1+0.5×2=3莫耳 3.
將0.4M硫酸溶液100毫升,再加水400毫升稀釋,混合均勻後,混合濃度為【0.08】M。 【解析】:溶質莫耳數=0.4×0.1=0.04莫耳 4.
6M的氫氧化鈉溶液500毫升,若溶液密度為1.2 克/cm3,請回答下列問題: (1)溶液中有【3】莫耳的溶質,相當於【120】克。(Na:23) (2)溶液的重量百分率濃度為【20】%。 【解析】:(1) 溶質莫耳數=6×0.5=3莫耳 5.
在2.5公升的硝酸水溶液中,共含有硝酸分子1.5×1022個,則: (1)水溶液中含硝酸分子【1.575】克;共有【0.025】莫耳的硝酸分子。 (2)溶液的莫耳濃度為【0.01】M。 【解析】:(1) 硝酸分子1.5×1022個=1.5×1022 ÷ 6×1023=0.025莫耳 6.
將3M的鹽酸稀釋為2M時,稀釋後溶液的體積和稀釋前溶液的體積比為【3:2】。 【解析】:溶質莫耳數=M×L=3×2=6莫耳 7.
請計算下列各題中含有溶質的重量為若干? (1) 0.5M、4升的碘化鉀:【332】克。 (2) 1.5M、400毫升的碳酸鈉:【63.6】克。 (3) 4M、20毫升的硝酸銀:【13.6】克。 (4) 2 M、500毫升的硫酸:【98】克。 【解析】:(1) 8.
小寶將2M氫氧化鈉溶液200毫升裝於燒杯中,不慎倒翻只剩一半,當她再加水至200毫升時: (1)溶液的莫耳濃度變為【1】M。 (2)將此溶液取出 50 毫升,其中含有【2】克的溶質。 【解析】: 9.
將原為12M的硫酸倒掉1/2體積後加滿水,再倒掉3/4體積後再加滿水,再倒掉1/2體積,最後濃度為【1.5】M。 【解析】: 10.
將一瓶糖水倒掉1/5體積後再加滿水,濃度變為0.4M,則糖水原來濃度為【0.5】M。 【解析】: 11.
將一瓶硫酸倒掉1/2體積後再加滿水,再倒掉1/2體積後再加滿水,再倒掉1/2體積後再加滿水,若最後濃度為0.5M,則原有的濃度為【4】M。 【解析】: 12.
欲將4M的硫酸溶液250毫升稀釋成1M,需加入【750】毫升的水。 【解析】: 13.
0.1M的氫氯酸10毫升,用水稀釋成100毫升後,莫耳濃度變為【0.01】M。 【解析】: 14.
甲燒杯含3M硝酸HNO3 400㏄,乙燒杯含5M的硝酸HNO3 600 ㏄ ,則:(N 的原子量為 14 )
(1)
甲燒杯中含純硝酸【1.2】莫耳,乙燒杯中含純硝酸【189】克。
(2)
將甲乙兩杯混合後,若總體積不增減,則混合液中硝酸的總莫耳數為【4.2】莫耳。
(3)
混合後的莫耳濃度為【4.2】M。
(4)
今將混合液取出200毫升,則含硝酸分子【0.84】莫耳,共有硝酸分子【5.04×1023】個。 【解析】: 15.
重量百分率濃度 90 %、密度1.6 g/㎝3的氫氧化鈉溶液 50 毫升,加水稀釋成 2 公升,則稀釋後的莫耳濃度為【0.9】M。 (Na:23) 【解析】: 16.
欲配製0.4 M 的HNO3
500毫升,需消耗重量百分率濃度 63 %、密度 2 克/㎝3的 HNO3溶液【10】毫升。 【解析】: 1.
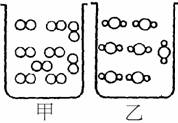
(1)
若兩杯溶液的體積相等,則【甲】杯所含的莫耳數較多。
(2)
若兩杯底面積相同,且兩杯溶液的高度比=3:2,則【乙】杯的莫耳濃度較大。
(3)
若兩杯溶液的重量相等,則【乙】杯重量百分率較大。 【解析】: |