|
|
|||||||||||||||||||||||||||||||||||||||||||||||
|
元素活性的大小:
鉀>鈉>鈣>鎂>鋁>碳>鋅>鉻>鐵>錫>鉛>氫>銅>汞>銀>鉑>金
K Na Ca Mg Al C
Zn Cr Fe Sn Pb H
Cu Hg Ag Pt Au (一)氧化和還原: A、
氧化:(1)物質和氧【化合】的過程,稱為氧化。 B、
還原:(1)氧化物中的元素和氧【化合】的過程,稱為還原。 C、
氧化還原反應: (1)
活性大的元素取代活性小的元素,使活性小的元素和氧脫離,稱為【氧化還原】反應。 (2)
此種反應方式必定【氧化】反應和【還原】反應同時存在。 (3)
活性小的元素不能取代活性大的元素。 (4)
產生氧化反應的物質稱為【還原劑】;產生還原反應的物質稱為【氧化劑】。
(5)
若A>B,則:
A + BO→ B + AO D、
實例: (1)
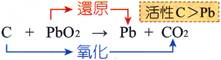
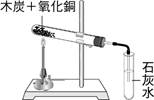
碳粉加入二氧化鉛混合後,以石棉紙包住,在火焰上加熱的實驗中,則: 反 應 方程式:【C+2PbO2 à 2Pb + CO2】。 元素活性大小:【C>Pb】
氧化物的活性大小:【CO2<PbO】。 碳粉的顏色為 【黑】色; 二氧化鉛粉末的顏色為【黃】色。 氧 化 反 應:【CàCO2】 還原反應:【PbOàPb】。 氧 化 劑:【PbO】
還 原 劑:【C】。
(2)
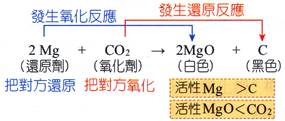
鎂帶在二氧化碳中燃燒,會產生白色的氧化鎂及黑色的碳粒子 反 應 方 程 式:【2Mg+CO 氧 化 反 應:【MgàMgO】 還原反應:【CO 還 原 劑:【Mg】
氧 化 劑:【CO2】。 【Mg】被【CO2】氧化成【MgO】;【CO2】被【Mg】還原成【C】。
(3)
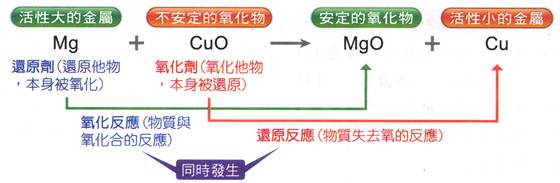
鎂帶和氧化銅反應產生白色的氧化鎂及赤紅色的金屬銅。 反 應 方 程 式:【Mg+CuO à Cu+MgO】。 氧 化 反 應:【MgàMgO】 還原反應:【CuOàCu】。 還 原 劑:【Mg】
氧 化 劑:【CuO】。 【Mg】被【CuO】氧化成【MgO】;【CuO】被【Mg】還原成【Cu】。 此反應結束後,氧化銅的顏色由【黑】色轉變成【紅】色
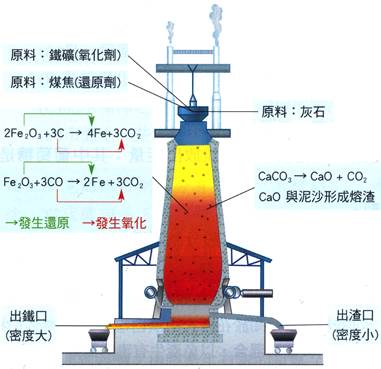
(二)鐵礦的冶煉: A、
原料:【鐵礦(Fe2O3)】、【煤焦(C)】、【灰石(CaCO3)】 B、
煉鐵裝置:【高爐】 C、
反應方程式: 2Fe2O3 + Fe2O3 + Fe2O3 + 3CO →2Fe +3CO2 CaCO3 → CaO + CO2 CaO + SiO2→ CaSiO3 D、
還原劑:【煤焦(C)】、【一氧化碳(CO)】。 E、
灰石的作用: (1)
除去鐵礦中的雜質,並防止鐵再氧化。 (2)
灰石分解後的【石灰(氧化鈣,CaO)】和鐵礦中的雜質作用,形成【熔渣(偏矽酸鈣CaSiO3)】,為液體, (3)
因為密度【小】,在熔鐵中上浮,因此出渣口較【高】。 (4)
熔渣可作為【水泥】的原料。 (三)鐵的種類: A、生鐵: (1)
由高爐所煉得最初的鐵為【生鐵】,又稱為【鑄鐵】。 (2)
含碳量最【大】,因此質脆,硬度大,凝固時體積略【膨脹】。 (3)
可鑄造模具,或鐵管。 B、熟鐵: (1)
生鐵經過鍛燒後,除去部分的碳,得到較純的鐵。 (2)
含碳量最【小】,質軟,硬度小,容易煅接,又稱為【煅鐵】。 (3)
可作為一般鐵釘、鐵絲的材料。 C、鋼鐵: (1)
含碳量介於【生鐵】和【熟鐵】之間。 (2)
兼有【生鐵】和【熟鐵】的特點,適合鑄造和鍛接,彈性最佳。 (3)
一般作為鋼筋、鋼釘等物質的材料。 比較:生鐵、熟鐵、鋼鐵的含碳量由大至小為:【生鐵】>【鋼鐵】>【熟鐵】。
|
|
|
|
|
|
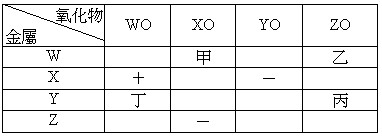
一、選擇題: ____1. 下列反應何者不是屬於氧化還原反應? 【答案】:【D】 【解析】: ____2. 關於煉鐵所產生的熔渣,下列敘述何者錯誤? 【答案】:【C】 【解析】: ____3. 煤焦與氧化鐵之反應如右: 【答案】:【C】 【解析】: ____4. 下列金屬氧化物,何者可用煤焦冶煉? 【答案】:【A】 【解析】: ____5. 將下列各組的混合物加熱,哪一組能發生氧化還原反應? 【答案】:【C】 【解析】: ____6. 工業上煉鐵,是在高爐(或鼓風爐)裡將含氧的鐵礦,以下列何種物質還原? 【答案】:【C】 【解析】: ____7. 高爐煉鐵時,爐頂放出的氣體主要含有: 【答案】:【C】 【解析】: ____8. 在2 Mg+CO2→C+ 【答案】:【B】 【解析】: ____9. 在Mg+CuO → Cu+MgO反應中,下列敘述何者不正確? 【答案】:【D】 【解析】: ____10.下列哪一種物質燃燒釀成火災時,不可以使用乾粉滅火器滅火? 【答案】:【C】 【解析】: ____11.將下列各組混合物加熱,預測不能發生氧化還原反應者為: 【答案】:【B】 【解析】: ____12.有關鐵元素的敘述,下列哪些為正確? 【答案】:【A】 【解析】: ____13.有關高爐煉鐵之敘述,哪一項不正確? 【答案】:【D】 【解析】: ____14.已知元素對氧的活性大小為Mg>Zn>Pb>Cu,下列化學反應式,何者正確? 【答案】:【D】 【解析】: ____15.下列何種物質最不易使鐵氧化? 【答案】:【A】 【解析】: ____16.下列有關氧化還原反應的性質,何項正確? 【答案】:【C】 【解析】: ____17.高爐中煉鐵的反應為: 【答案】:【C】 【解析】: ____18.Fe2O3+C → Fe+CO2(未平衡),試問12公斤的煤焦和足量的Fe2O3反應,約可煉得多少公斤的鐵?(Fe=56、C=12、O=16) 【答案】:【C】 【解析】: ____19.將點燃的鎂帶分別放入在裝有(甲)空氣、(乙)純氧、(丙)氮氣、(丁)二氧化碳的四個廣口瓶中,會使鎂帶繼續燃燒的共有幾瓶? 【答案】:【D】 【解析】: ____20.設A、B、C代表三種元素,AO、BO、CO分別代表其氧化物。AO+B → BO+A,AO+C → 無反應;依上列反應式判斷此三種元素對氧的活性順序何者正確? 【答案】:【A】 【解析】: ____21.在 【答案】:【A】 【解析】: ____22.下列哪一項反應不是氧化還原反應? 【答案】:【D】 【解析】: ____23. 【答案】:【B】 【解析】: ____24.W、X、Y、Z為四種金屬,WO、XO、YO、ZO為金屬氧化物,現以各種金屬與金屬氧化物相互作用,其中會產生反應者以「+」表示,不會產生反應者以「-」表示,結果如附表。則WO、XO、YO、ZO中,何者為最強的氧化劑? 【答案】:【D】 【解析】: ____25.四種金屬對氧的化學活性順序為:鈉>鋁>鐵>銅,此四種金屬與鹽酸作用只有銅無反應。在適當溫度下,下列哪一組可以發生氧化還原反應? 【答案】:【C】 【解析】: ____26.在CO2+ 【答案】:【C】 【解析】: ____27. (甲) H2+CaO;(乙) C+Fe2O3;(丙) Mg+ZnO。甲、乙、丙在高溫狀態下會發生氧化還原反應的是: 【答案】:【C】 【解析】: ____28.下列哪一項反應過程,必須加入氧化劑?(註:各式中僅列出主要反應,未平衡) 【答案】:【C】 【解析】: ____29.在CuO+H2
→ Cu+H2O的氧化還原反應中,何者為氧化劑? 【答案】:【A】 【解析】: ____30.將鐵礦、熔劑(灰石)與焦煤置於高爐中煉鐵,下列何者錯誤? 【答案】:【D】 【解析】: ____31.冶煉鐵礦時,在高爐內加入焦煤是作為: 【答案】:【B】 【解析】: ____32. (甲) C+2 PbO → 2Pb+CO2;(乙) Pb+CuO → Cu+PbO;(丙) 2 Mg+CO2 → C+2MgO,從上述三個反應式中可推知Pb、Cu、Mg三種金屬元素之活性大小順序為: 【答案】:【B】 【解析】: ____33.高爐煉鐵,一氧化碳與氧化鐵反應如右:Fe2O3+ 【答案】:【A】 【解析】: ____34.馬蓋先經實驗結果,歸納得知下列兩項事實:(1)焦煤不能用來還原鋁礦,但可用來還原銅礦和鐵礦。(2)不能用鐵罐填裝硫酸銅水溶液。如此,可知C、Al、Cu、Fe四元素的活性由大到小順序是下列哪一項? 【答案】:【D】 【解析】: ____35.將鋅片放入硫酸銅水溶液中,觀察到有反應發生,則關於此反應的敘述,下列何者正確? 【答案】:【B】 【解析】: ____36.在CuO+H2
→ Cu+H2O的氧化還原反應中,何者為還原劑? 【答案】:【B】 【解析】: ____37.在煉鐵的過程中,何者為還原劑? 【答案】:【D】 【解析】: ____38.下列何者不可能發生氧化還原反應? 【答案】:【D】 【解析】: ____39.將鐵礦、灰石與焦煤置於高爐中煉鐵,下列敘述何者錯誤? 【答案】:【B】 【解析】: ____40.下列何種物質既宣鑄造又宜 【答案】:【C】 【解析】: ____41.下列哪一種元素可在二氧化碳中繼續燃燒? 【答案】:【D】 【解析】: ____42.已知Na、Ca、Mg、C、Cu對氧的活性順序是:Na>Ca>Mg>C>Cu,下列四組物質,何者會發生氧化還原反應? 【答案】:【D】 【解析】: ____43.請完整的挑出下列正確的敘述: 【答案】:【C】 【解析】: ____44.下列有關煉鐵的敘述,哪一項錯誤? 【答案】:【A】 【解析】: ____45.下列敘述何者正確? 【答案】:【D】 【解析】: ____46.下列哪一反應不是氧化還原反應? 【答案】:【D】 【解析】: ____47.X、Y、Z三種金屬元素在空氣中的燃燒情形為:Y容易燃燒;X較不易燃燒;Z最不易燃燒;以XO、YO、ZO代表三種金屬的氧化物,下列各組反應,哪一組會發生反應? (A) Y和XO (B) X和YO (C) Z和XO (D) Z和YO 【答案】:【A】 【解析】: ____48.下列金屬氧化物與碳粉混合加熱後,何者不能得到金屬? 【答案】:【A】 【解析】: ____49.已知鈣(Ca)的活性大於銅(Cu),若無其他物質參與反應,則下列哪一組的物質,經混合加熱後,可發生氧化還原反應? 【答案】:【C】 【解析】: ____50.乾燥鎂粉和氧化銅混合加熱,容易得到銅和氧化鎂(Mg+CuO Δ─→ Cu+MgO),可知: 【答案】:【B】 【解析】: ____51.在下列變化中,哪種不能產生氧化鎂? 【答案】:【B】 【解析】: ____52.下列何者為氧化還原反應? 【答案】:【A】 【解析】: ____53.下列各情況,哪一種不能發生反應? 【答案】:【B】 【解析】: ____54.鎂帶在裝有二氧化碳的廣口瓶中燃燒,會在瓶子內壁附著碳粉,何者在此一氧化還原反應中做為還原劑? 【答案】:【A】 【解析】: ____55.下列何者無法當還原劑? 【答案】:【C】 【解析】: ____56.下列何者為氧化還原反應? 【答案】:【A】 【解析】: ____57.若已知甲為既宜鑄造又宜煅接的鐵;乙為含碳量最少、純度最高的鐵;丙為含碳量最高,質硬且脆的鐵,則甲、乙、丙分別為: 【答案】:【B】 【解析】: ____58.生鐵、熟鐵及鋼含碳量的大小為: 【答案】:【B】 【解析】: ____59.高爐中鐵的生成經由下面的反應:Fe2O3+ 【答案】:【B】 【解析】: ____60.下列何者不包含還原反應? 【答案】:【C】 【解析】: ____61.下列各項中,哪一項是還原劑的特性? 【答案】:【B】 【解析】: ____62.焦煤及燃燒生成的一氧化碳都可還原氧化鐵,其反應式依次是: 【答案】:【B】 【解析】: ____63. (甲) Al2O3+Cu;(乙) Cu+Al;(丙) Al+CuO;(丁) Al2O3+CuO。 【答案】:【A】 【解析】: ____64.把點燃的鎂帶放進二氧化碳的集氣瓶中發現鎂帶繼續燃燒,反應後,瓶壁上有黑色斑點附著。請問下列敘述何者錯誤? 【答案】:【B】 【解析】: ____65.X、Y、Z分別代表三種元素,XO、YO、ZO代表它們的氧化物,如有下列反應發生:Y+X → YO+Z;X+ZO→XO+Z,則它們的活性大小順序為何? 【答案】:【B】 【解析】: ____66.點燃的鎂帶發出強烈的白光,放入CO2瓶內,則下列敘述何者正確? 【答案】:【B】 【解析】: ____67.鎂帶可在二氧化碳中繼續燃燒,下列敘述何者錯誤? 【答案】:【C】 【解析】: ____68.在鎂與氧化銅的反應:Mg+CuO→MgO+Cu,下列敘述何者正確? 【答案】:【A】 【解析】: ____69.鐵礦、灰石、焦煤是煉鐵的主要原料;加入灰石目的,是與礦石中的泥沙作用生成: 【答案】:【A】 【解析】: ____70.下列哪一項反應過程,必須加入還原劑? 【答案】:【B】 【解析】: ____71.冶煉鐵礦時,加入灰石的主要目的為下列何者? 【答案】:【D】 【解析】: ____72. (甲) CO2+2 Mg → C+2 MgO;(乙) Fe2O3+3 CO 【答案】:【A】 【解析】: ____73.X、Y、Z三種金屬元素在氧氣中燃燒的情形為:Y最容易燃燒,X較不易燃燒,Z最不易燃燒;以XO、YO、ZO代表三種金屬的氧化物,若將下列各組混合物加熱,哪一組會發生氧化還原反應? 【答案】:【A】 【解析】: ____74.冶煉金屬時常用碳當還原劑,其原因下列何者錯誤? 【答案】:【C】 【解析】: ____75.已知鈉、鋅、銅對氧的活性順序是:鈉>鋅>銅,則下列哪一組混合物,加熱後可發生氧化還原反應? 【答案】:【B】 【解析】: ____76.將點燃的鎂帶放入裝有二氧化碳的廣口瓶中,反應後會在瓶子內壁附著何種物質? 【答案】:【A】 【解析】: ____77.在鋼中加入何種成分可以大幅提高鋼的硬度? 【答案】:【D】 【解析】: ____78.鐵礦、焦煤、熱空氣、熔劑是煉鐵的四大要件,以上何者是擔任還原劑的角色? 【答案】:【B】 【解析】: ____79.下列哪一組混合物,加熱後可發生氧化還原反應? 【答案】:【D】 【解析】: ____80. (甲)氧化鎂;(乙)氧化鋅;(丙)氧化銅,三種氧化物與碳作用何者最活潑? 【答案】:【C】 【解析】: ____81.在氧化還原反應中,下列何者錯誤? 【答案】:【D】 【解析】: ____82.鋅粉與氧化銅粉末在隔絕空氣條件下混合加熱反應如下: 【答案】:【D】 【解析】: ____83. 【答案】:【B】 【解析】: ____84. 【答案】:【A】 【解析】: ____85.鋁熱劑點燃後,能生成熔融狀態的鐵,可用來修補鐵軌,其成分可能為: 【答案】:【B】 【解析】:
|
|
|
|
|
已知Ca+ZnO→Zn+CaO,Cu+ZnO→不會反應,則: 1. 日常生活中,氧是最常接觸到的【氧化劑】,碳則是常見的【還原劑】。(請填氧化或還原) 2. 鐵礦製成鐵,可依右列化學反應式反應得: ( )1. 在此反應中Fe2O3的角色是:【A】 ( )2. 50公斤的氧化鐵與足量的碳反應,所產生的鐵其質量與下列何值最接近?【A】 3. 鐵礦煉鐵高爐中的煤焦在空氣不足下燃燒會產生一氧化碳,一氧化碳也可作為還原劑,其反應式如下(未平衡)a
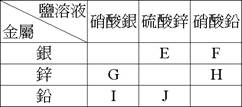
Fe2O3+b CO → c Fe+d CO2其平衡係數和a+b+c+d=【9】。 4. ( )1. 則右表中有鉛被取代出來的反應為:【C】 ( )2. 承上題,附表中沒有化學反應發生者為:【B】 5. ( )1. 下列何者不是從爐頂的受料斗中放入的原料?【C】 ( )2. 下列哪兩種物質皆可做為煉鐵時的還原劑?【B】 ( )3. 冶煉鋼鐵時,加入灰石的作用是:【C】 6. 小明做了下列實驗的步驟: ( )1. 鎂可在CO2中燃燒是因鎂和碳的活性何者較大?【A】 ( )2. 乙步驟表示燃燒產物溶於水後形成:【C】 ( )3. 甲步驟的化學反應式:2 Mg+CO2 → C+2 MgO,下列何者為氧化劑?【B】 ( )4. 丙步驟中的黑色物質是:【C】 7. (1)
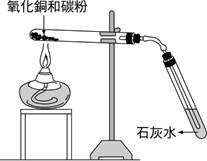
試管中產生的化學變化之反應式:【2CuO+C→2Cu+CO2】。 (2)
上述反應中,還原劑為【碳C】。 (3)
石灰水是為了檢測【CO2】。 (4)
實驗結束後應如何收拾該實驗裝置?【B】 (5)
煉鐵時,加入的灰石,學名為【碳酸鈣】,在高爐中受熱會分解為【氧化鈣CaO】和【二氧化碳CO2】氣體。(請填學名) 8. 碳粉和氧化銅粉末隔絕空氣加熱產生的反應,回答下列問題:(Cu=64、O=16、C=12) (1)
(2)
反應後產生的有色生成物是【Cu】。 (3)
此反應的氧化劑是【氧化銅CuO】。 9. C+2 CuO→CO2+2 Cu,此反應的氧化劑為【氧化銅CuO】;還原劑為【碳C】。 10. (1)
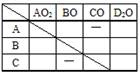
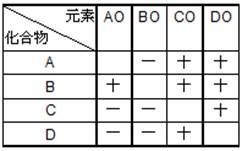
右表中『B+AO』是否有反應?【是】。
(2)
『A+CO』反應中,產物為【C+AO】;何者為氧化劑【CO】,何者為還原劑?【A】。 (3)
A、B、C、D 四元素中,活性的大小依序為【B>A>D>C】。 (4)
AO、BO、CO、DO 四元素之氧化物其活性大小依序為【CO>DO>AO>BO】。 (5)
A、B、C、D 中何者為最強的還原劑?【B】。 (6)
AO、BO、CO、DO中,何者為最強的氧化劑?【CO】。 (7)
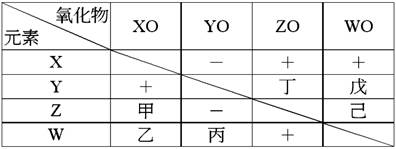
AO、BO、CO、DO 中,何者最易起變化?【CO】。何者最安定?【BO】。 11. ( )1. X、Y、Z、W四種金屬元素活性由大至小依次為:【D】 ( )2. 如表中所示,甲、乙、丙、丁、戊、己中有反應者為:【B】 ( )3. XO、YO、ZO、WO四種金屬元素的氧化物其活性大小依序為:【B】 ( )4. X、Y、Z、W四種金屬之中,有最強還原作用的是:【B】 12. X,Y,Z,W代表四種元素,XO,YO,ZO,WO代表氧化物,依據反應回答下列問題: (1)
求對氧的活性由大至小依序為:【Z>Y>X>W】。 (2)
求氧化物的安定性由大至小依序為:【ZO>YO>XO>WO】。 13. CuO+Mg→Cu+MgO反應中【鎂Mg】被氧化,【氧化銅CuO】被還原; 14. 下列變化,(A)C→CO2 (B)Fe2O3→Fe (C)CuO→Cu (D)Mg→MgO;請回答下列問題: (1)
上述反應中何者是氧化?【AD】;何者是還原?【BC】。 (2)
上述反應中何者需加入氧化劑?【AD】;何者需加入還原劑?【BC】。 15. 三瓶內分別裝有無色的氦氣、二氧化碳和氧氣。點燃鎂帶分別放入各瓶,發現在A、B瓶中繼續燃燒,在C瓶中熄滅。在A瓶內有黑色物質和白色物質發生;在B瓶內只有白色物質產生。試回答下列問題: (1)
A瓶內裝的是什麼氣體?【CO2】。(填化學式) (2)
B瓶內裝的是什麼氣體?【O2】。(填化學式) 16. A、B、C、D代表四種元素,AO、BO、CO、DO代表氧化物,若A與BO、CO、DO無反應,B僅與AO反應,D可與CO反應,則四種元素對氧活性由大至小依次為【D>C>B>A】。 17. 某生欲覾察鎂、碳、鉛等元素是否由氧化物中取代其他元素出來,作了下列實驗探討: (1)
將木炭粉與氧化鉛混合均勻後,以石棉紙包住,以坩堝鉗夾住,在火焰中加熱後,觀察結果,則有金屬光澤的【鉛Pb】生成,由此可推測【碳C】對氧的活性大於【鉛Pb】。 (2)
以坩堝鉗夾緊鎂帶,點燃後,立刻插入裝有二氧化碳的集氣瓶中,則鎂帶【可以】燃燒,作用完成後,生成白色的【氧化鎂MgO】,旦集氣瓶壁附有很多【黑色】斑點的【碳C】。 (3)
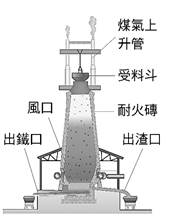
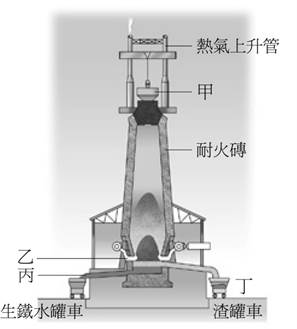
寫出上題的方程式:【2Mg+CO2→C+2MgO】。可知鎂和碳對氧的活性為【Mg>C】。 18. 如圖為工業上煉鐵的高爐裝置。試回答下列問題: (
)1. (
)2.將鐵礦、灰石與煤焦置於高爐中煉鐵,下列敘述何者錯誤?【B】 (
)3.赤鐵礦煉製鐵之過程中,涉及 【答案】:【10公斤】 【解析】: (
)4.從高爐中煉得的鐵由何處流出?【C】 (
)5.從高爐中煉得的鐵是:【A】 (
)6.生鐵、熟鐵及鋼含碳量的大小為:【B】 (
)7.鐵礦、灰石、煤焦是煉鐵的三種主要原料;加入灰石的目的,主要是與礦石中的泥沙作用生成:【A】 (
)8.工業上煉鐵,是在高爐(或鼓風爐)裡將含氧的鐵礦,以下列何種物質還原?【C】 (
)9.將鐵礦製成鐵,可依右列之方程式反應而得: (
)10.承上題, (
)11.高爐煉鐵得Fe2O3+CO → Fe+CO2 反應中,反應式的平衡係數為:【C】 (
)12.下列有關煉鐵的技術,哪一項錯誤?【D】 19. A、B、C三元素與氧化物AO、BO、CO間反應結果如表(+為有反應,-為沒有反應),則: (1)
A+CO是否有反應?【】。 (2)
乙中應填入 "+" 或”-”? 【】。 (3)
A、B、C的活性由大而小為【】。 (4)
氧化物最安定的是【】。 20. 已知活性大的金屬,可與活性小的金屬氧化物發生反應,附表為W、X、Y、Z四種金屬,WO、XO、YO、ZO為其金屬氧化物,小榮以各金屬和不同金屬的氧化物反應,結果如右表:(+:代表有反應,-:代表無反應) ( )1. ( )2. 由右表可知X與Z的活性大小為:【A】 ( )3. 由右表可知Y與X的活性大小為:【A】 ( )4. 如欲比較各金屬的活性大小,小榮尚需再做下列哪一項實驗?【B】 ( )5. 承(4),若選取之實驗結果為+,可得W、X、Y、Z四種金屬的活性大小順序為:【B】
|
|
|
|
|
|
|
|
| |