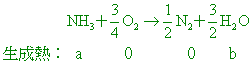|
( )1.
已知H2O(l) → H2(g)+ 【答案】:(D) 【解析】:H2O(L)
→H2(g)+(1/2)O2(g) ΔH=285 kJ [ H2(g)+(1/2)O2(g) →H2O(L) ΔH=-285 kJ ( )2.
已知氨與水的草耳生成熱分別為a kJ、b kJ,則1莫耳氨在氧氣中完全反應生成氮氣和水的反應熱為多少kJ? 【答案】:(D) 【解析】: ( )3.
已知二氧化碳、水及乙烯的莫耳生成熱分別為a kJ、b kJ、c kJ,則乙烯(C2H4)的莫耳燃燒熱為多少kJ? 【答案】:(A) 【解析】: ( )4.
已知CH4(g)的莫耳生成熱為-75千焦,H2O(g)的莫耳生成熱為-287千焦,C(s)的莫耳燃燒熱為-394千焦,則CH4(g) + 2O2(g)
→ CO2(g) + 2H2O(L) 的ΔH為何? 【答案】:(A) 【解析】:C(s)的燃燒熱=二氧化碳CO2的生成熱=-394(KJ) ( )5.
下列有關反應熱的說明,何者正確? 【答案】:(D) 【解析】:(A) H2的莫耳燃燒熱=H2O的莫耳生成熱,兩者為等值同號。 |
|
( )6.
有關反應熱的敘述,下列何者正確? 【答案】:(C) 【解析】:(A)生成熱的反應物是在常溫常壓下自然界的元素物質,不是單一原子,因此反應式 ( )7.
有一暖暖包內含100毫升的水,暖暖包中另有一塑膠袋,內裝氯化鈣固體。使用時稍為用力敲打暖暖包,使其中的塑膠袋破裂,讓水與氯化鈣混合。已知氯化鈣的溶解熱為-84.0 kJ/mol,而水的比熱為4.20 Jg-1K-1。假設氯化鈣的比熱甚小可以忽略,而氯化鈣溶解所釋出的熱量,完全由100毫升的水所吸收。若在阿里山上,取出一個 【答案】:(C) 【解析】:水的比熱=1cal/g℃=1Kcal/Kg℃=4.2J/g℃ 100mL的水質量為100克 ( )8.
已知N2(g)+2O2(g) ® 2NO2(g)-67.6 kJ,有關左列反應式的敘述何者正確? 【答案】:(D) 【解析】:N2(g)+2O2(g) ® 2NO2(g)-67.6 kJ [ N2(g)+2O2(g) +67.6 kJ® 2NO2(g) ( )9.
在標準狀況下,已知CO2的標準莫耳生成熱為-393.6 kJ,且已知: 【答案】:(C) 【解析】: ( )10.
下列有關反應熱的敘述,何者正確? 【答案】:(D) 【解析】:(A) |
|
( )11.
下列哪些反應熱是莫耳燃燒熱? 【答案】:(E) 【解析】:(A)C(S)的燃燒熱是完全燃燒,產生CO2(g),不是CO(g)。 ( )12.
關於熱化學反應式,C(s)+O2(g) ® CO2(g),ΔH=-394 kJ,下列敘述何者正確? 【答案】:(B) 【解析】:C(s)+O2(g) ® CO2(g),ΔH=-394 kJ,ΔH為負值,因此為放熱反應。 ( )13.
在 【答案】:(B) 【解析】: ( )14.
下列哪個反應熱發生後,反應熱ΔH必為負值? 【答案】:(C) 【解析】:(A)大部分固體的溶解熱為吸熱,但部分固體溶解為放熱。 ( )15.
在1 atm, 【答案】:(C) 【解析】:元素的生成熱為零,因此氫氣H2、氧氣O2、斜方硫S8、白磷P4、石墨C、鎂帶Mg的生成熱為零。但是元素一般的燃燒熱不為零,僅不可燃的物質燃燒熱為零,因此各項中僅氧氣O2的燃燒熱為零。 |
|
( )16.
下列各反應中何者的能量變化最小? 【答案】:(B) 【解析】:(A) H2(g)
+ ( )17.
下列何項反應會放出最多的熱量? 【答案】:(B) 【解析】:氣體的熱含量比液體的熱含量多,選項中的方程式為燃燒方程式,必為放熱反應。因此(B)放熱最多。 ( )18.
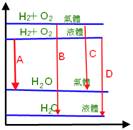
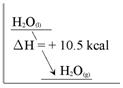
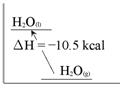
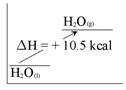
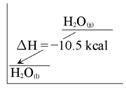
下列四圖中何者為H2O(l) + 10.5 kcal →
H2O(g) 的熱含量變化簡圖?(橫軸代表變化過程,縱軸代表熱含量變化) 【答案】:(C) 【解析】:水H2O(液體)→H2O(氣體),為吸熱反應,吸熱10.5KJ。 ( )19.
CO2(g)、H2O(l)及C3H8
(g) 之莫耳生成熱為ΔH1、ΔH2及ΔH3,試問C3H8之莫耳燃燒熱為何? 【答案】:(D) 【解析】: ( )20.
CO2(g) 的莫耳生成熱與C(s) 的莫耳燃燒熱有何關係? 【答案】:(A) 【解析】:碳C的燃燒熱和二氧化碳生成熱為同一反應方程式,兩者等值同號。 |