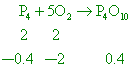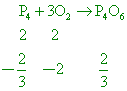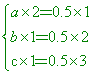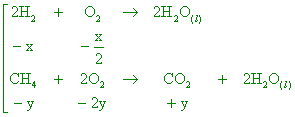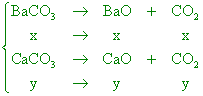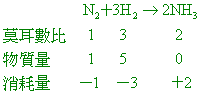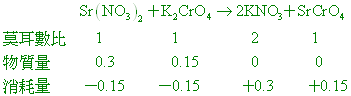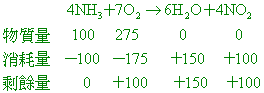|
( )1.
金屬鎂與鹽酸反應會生成氫氣,在25℃ 、1大氣壓的情況下,過量的鎂與5.00
M的鹽酸100 mL完全反應時,則可產生多少升的氫氣? 【答案】:(D) 【解析】:Mg+2HCl→MgCl2+H2 5.00
M的鹽酸100 mL=5x0.1=0.5莫耳 ( )2.
0.42克的化合物 【答案】:(A) 【解析】:MH2+2H2O→M(OH)2+2H2 0℃、1大氣壓下,1莫耳的氣體有22.4升 ( )3.
容積不同的甲、乙兩個容器中分別置入磷與氧各2莫耳,在不同狀況下分別以下列方式進行充分反應: 【答案】:(C) 【解析】: ( )4.
超導體為具有零電阻及反磁性的物質,以 【答案】:(B) 【解析】: ( )5.
定壓下,使氫、甲烷及氧之混合氣體100 mL完全燃燒後通過無水過氯酸鎂中,然後使溫度恢復至室溫而測得氣體體積為70
mL,再通入氫氧化鉀水溶液中,測得氣體體積為64 mL,則最初氫與甲烷之體積比為 【答案】:(A) 【解析】:2H2+O2→2H2O CH4+2O2→CO2+2H2O
|
|
( )6.
粉末氯酸鉀(KClO3)隨加熱條件之不同而產生不同生成物,下列四種氯酸鉀反應中,其重量減少約等於13.1%的反應為何者?(K 【答案】:(D) 【解析】:化學反應前後質量應守恆,及反應前質量=反應後質量 ( )7.
取9.0克的純鋁溶於鹽酸中,將生成的氫氣通過灼熱的氧化銅中,收集所得的純銅,放入硝酸銀溶液,經過的反應如下:(原子量:Al 【答案】:(C) 【解析】:9克的Al莫耳數= ( )8.
在標準狀態下,將2莫耳的氯酸鉀(KClO3)完全分解,則可產生多少升的氧?
【答案】:(E) 【解析】: ( )9.
【答案】:(A) 【解析】:CaCO3分子量=100, 100克CaCO3=1 mol, ( )10.
某硫酸銅晶體,加熱後得無水硫酸銅 【答案】:(B) 【解析】:CuSO4分子量=64+32+16x4=160 160÷0.82=195(化合物的分子量) |
|
( )11.
BaCO3和CaCO3的混合物6.94克,經加熱使其放出CO2後得BaO和CaO的混合物4.74克。則原混合物中含有BaCO3多少克?(Ba 【答案】:(C) 【解析】:假設BaCO3有x莫耳,CaCO3有y莫耳;
( )12.
水電解的反應式: 【答案】:(A) 【解析】: ( )13.
【答案】:(C) 【解析】:KClO4分子量=39+35.5+16x4=138.5 27.7÷138.5=0.2莫耳 ( )14.
10 g的碳酸鈣加熱完全分解,可得氧化鈣多少克?(Ca 【答案】:(A) 【解析】:CaCO3分子量=40+12+16x3=100 CaO分子量=40+16=56克 ( )15.
10克的X與5克的Y,兩者反應產生Z,反應後剩下4克的X、2克的Y,試問該反應之反應式為何?(X 【答案】:(A) 【解析】:X消耗=10-4=6克 Y消耗=5-2=3克, Z質量=6+3=9克 |
|
( )16.
設加熱不純的 【答案】:(D) 【解析】:CaCO3→CaO+CO2 減少的質量=產生CO2的質量 ( )17.
取 【答案】:(C) 【解析】:N2分子量=14x2=28, H2分子量=1x2=2 NH3分子量=14+1x3=17
( )18.
取0.20升之1.5M的Sr(NO3)2(aq)與0.30升之0.5M的K2CrO4(aq)混合,當 【答案】:(A) 【解析】:Sr(NO3)2(aq)的莫耳數=1.5x0.2=0.3莫耳, K2CrO4(aq)的莫耳數=0.5x0.3=0.15莫耳,
( )19.
在200 【答案】:(D) 【解析】:定溫定壓下,氣體反應的體積比=莫耳數比,反應式:4NH3+7O2 → 6H2O+4NO2
( )20.
【答案】:(A) 【解析】:設溶解的金屬皆為1克,則 |
|
( )21.
冬天時不宜戴銀戒指去硫磺溫泉區,此因銀與溫泉氣體( 【答案】:(D) 【解析】:Ag莫耳數= ( )22.
某碳氫化合物2.2克,完全燃燒後產生6.6克二氧化碳,則此化合物最可能之化學式為 【答案】:(D) 【解析】:C質量= ( )23.
水楊酸( 【答案】:(B) 【解析】:水楊酸分子量=12x7+1x6+16x3=138 |