|
( )1.
物質X燃燒時的化學反應式為: 【答案】:(C) 【解析】:先平衡O(右邊8個O),再平衡X(左邊2個X) [ d=2 ( )2.
將右列的反應式:NH3+O2→NO2+H2O
平衡後,其係數分別為何?
【答案】:(B) 【解析】:先平衡H(做邊3個H,右邊2個H),再平衡N(左邊2個N), ( )3.
物質X燃燒時的化學反應式為 【答案】:(C) 【解析】:先平衡O(右邊8個O),再平衡X(左邊2個X) [ d=2 ( )4.
銅片與稀硝酸加熱產生硝酸銅、一氧化氮與水,反應式如下: 【答案】:(C) 【解析】:先平衡H(右邊2個H),得 aCu+2HNO3→bCu(NO3)2+cNO+1H2O ( )5.
有25克甲物質、5克乙物質、10克丙物質混合加熱,使它們發生化學反應,經分析反應後,混合物中含10克甲、21克丙,還含有一種新物質丁。若甲、乙、丙、丁的式量分別為30、20、44、18,並用A、B、C、D分別表示它們的化學式,則它們之間所發生化學反應的方程式是 【答案】:(D) 【解析】:反應前後比較,甲消耗25-10=15克,乙用盡=5克,丙產生11克, |
|
( )6.
甲烷燃燒不完全時,產生CO及 【答案】:(B) 【解析】:先平衡C(左邊1個C),再平衡H(左邊4個H),再平衡O(右邊2+1=3個O) ( )7.
有關 【答案】:(A) 【解析】:同溫同壓下氣體反應的體積成簡單整數比,但是在常溫下,水H2O為液態,不遵守氣體反應體積定律,除非再100℃以上成為水蒸氣H2O(g),才能成立。 ( )8.
取某醇類(CnH2n+2O)若干克,完全燃燒後,生成88克CO2與45克H2O,則此醇類分子式為何? 【答案】:(C) 【解析】:CO2分子量=44,H2O分子量=18,88÷44=2莫耳, 45÷18=2.5莫耳 ( )9.
反應:甲 【答案】:(A) 【解析】:反應完後甲耗盡而乙剩下2克,因此甲消耗8克,乙消耗14-2=12克,丙產生16克, ( )10.
酒醉駕車是造成臺灣交通事故的主因。交通警察利用酒精(乙醇)吹氣濃度試驗檢測駕駛者體內酒精含量,所依據的化學原理是乙醇在酸性條件下被氧化成乙酸,同時二鉻酸根( 【答案】:(B) 【解析】:xK2Cr2O7+yH2SO4+3CH3CH2OH→2Cr2(SO4)3+zK2SO4+3CH3COOH+11H2O |
|
( )11.
完全燃燒X莫耳正丁烷( 【答案】:(D) 【解析】:正丁烷的化學式為C4H10,會產生4個CO2, ( )12.
下列化學反應式 【答案】:(C) 【解析】:先平衡K(左邊2個K),再平衡Cr(左邊2個Cr), ( )13.
完全燃燒X莫耳正丁烷得Y莫耳二氧化碳時,下列X與Y間的關係,何者正確? 【答案】:(D) 【解析】:正丁烷的化學式為C4H10,會產生4個CO2, ( )14.
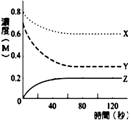
【答案】:(B) 【解析】:如圖,X濃度:0.8M→0.6M,Y濃度:0.7M→0.3M,X濃度:0M→0.2M, ( )15.
在一密閉容器內,等莫耳的X2和Y2進行下列反應: 【答案】:(A) 【解析】:X2+3Y2→2XY3,反應過程消耗1莫耳X2,消耗3莫耳Y2,同時產生2莫耳XY3, |
|
( )16.
利用代數法平衡下列反應式: 【答案】:(B) 【解析】:先平衡Al,再平衡電荷(右邊1個負電),再平衡(右邊4個O), ( )17.
平衡下列反應式後: 【答案】:(C) 【解析】:先平衡K(左邊2個K),再平衡Cr(左邊2個Cr),再平衡O(左邊7個O), ( )18.
化學反應:aPb(OH)(CH3COO)+bCO2→xPb3(OH)2(CO3)2+yH2O+zPb(CH3COO)2
【答案】:(B) 【解析】:Pb(OH)(CH3COO)+CO2→1Pb3(OH)2(CO3)2+H2O+Pb(CH3COO)2 ( )19.
有關方程式 【答案】:(C) 【解析】:方程式的平衡係數代表化學反應時,反應物的消耗量與生成物的產生量之間的關係, ( )20.
超導體為具有零電阻及反磁性的物質。現以 【答案】:(D) 【解析】:YBa2Cu3Ox包含(1/2)Y2O3+2BaCO3+3CuO |
|
( )21.
有關反應式 【答案】:(A) 【解析】:先平衡Cr(左邊2個Cr),再平衡O(左邊7個O),再平衡H(右邊7x2=14個H), ( )22.
平衡反應式 【答案】:(C) 【解析】:先平衡Mg(左邊3個Mg),再平衡O(右邊3x2=6個O),再平衡N(左邊2個N), ( )23.
物質X燃燒時的化學反應式為: 【答案】:(C) 【解析】:X+2 O2→CO2+H2O,X中含C、含H, ( )24.
以最簡整數平衡 【答案】:(E) 【解析】:先平衡C(左邊6個C),再平衡H(左邊12個H),再平衡O(右邊6x2+6=18個O), |