|
|
||||||||||
|
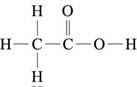
(一) 化學式的意義: A、 凡用元素符號和簡單數字來表示物質組成的式子,稱為化學式。 B、 常見化學式有實驗式、分子式、結構式、示性式及電子點式等。 C、 電子點式可以將分子內的價電子分布情形表示出來。 D、 醋酸的化學式
(二) 實驗式: A、 表示純物質組成的最簡單化學式,稱為實驗式;它僅能表明物質內所含原子種類與不 B、 不同的化合物,可以有相同的實驗式。 C、 實驗式內各元素之原子量總和,稱為「實驗式量」,簡稱「式量」。 D、
實驗式相同的物質,重量百分組成必相同。 E、
實驗式相同的兩不同化合物,等重時,具有相同的原子數,但是不同的分子數目。 F、
實驗式相同的兩不同化合物,等重的有機物完全燃燒時,需氧量相同,生成CO2的質量也相同。 G、 常以實驗式表示的非分子物質: (1). 金屬元素(金屬晶體):如鈉(Na)、銅(Cu)、鐵(Fe)、銀(Ag)等。 (2). 網狀固體:如金剛石(C)、石墨(C)、矽(Si)、金剛砂(SiC)、二氧化矽(SiO2)等。 (3). 離子化合物:如食鹽(NaCl)、氯化銨(NH4Cl)、氫氧化鈉(NaOH)、硝酸鉀(KNO3)等。 【註】:金屬晶體、離子化合物、網狀共價固體都是由原子或離子堆積而形成兩度或三度空間的巨大結構,沒有特定的原子數目及大小,沒有具體的分子存在其中,因此僅知晶體內原子的種類及比例,故以簡式表示。 (三) 分子式: A、 分子式是表示分子結構物質每一分子中所含原子種類及數目的化學式。 B、 乙醇C2H5OH的分子式為C2H6O,甲醚CH3OCH3的分子式為C2H6O,兩者有相同的分子式,但是結構排列不相同,因此性質不相同,稱為同分異構物。 C、 乙醇和甲醚的分子式相同,因此簡式相同,但由於排列不同,因此示性式不同,結構式不同,不是相同物質。 D、 分子式=(實驗式)n,分子量=(式量)xn。 (1) 常態下的氣體: 甲、 元素:氫氣(H2)、氧氣(O2)、氮氣(N2)、氟氣(F2)、氯氣(Cl2)及鈍氣(惰性氣體)。 乙、 化合物:CO、CO2、NO、NO2、SO2、SO3、CH4、C2H6…等。 (2) 一些非金屬元素:芙(C60)、黃磷(P4)、硫磺(S8)、溴(Br2)、碘(I2)…等。 (3) 常見的酸及有機物: 甲、 無機含氧酸(HmXOn):如H2SO4、HNO3、H3PO4、H2CO3…等。 乙、 非金屬的氫化物:如HCl、HBr、H2S、HCN…等。 丙、 有機化合物:如C6H12O6、C2H5OH、CH3COOH…等。 (四) 結構式: A、
表示分子內所含原子種類、數目和排列方式的化學式,但不能表示此分子真正的立體結構。 B、
甲烷(CH4)之結構式為,但實際上4個氫原子並非在同一平面上,真正的分子形狀為正四面體。 C、
丙醛C2H5CHO,及丙酮CH3COCH3,兩者的分子式皆為C3H6O,但結構排列不相同,其示性式及結構式都不同,兩者互為同分異構物。 D、
同分異構物有相同的分子式,相同的簡式,相同的重量百分組成;但具有不同的示性式,不同的結構式,不同的物理性質及化學性質。 E、
分子模型可用來表示分子立體結構,使我們對分子形狀有更正確的認知。 (五) 示性式: A、
示性式是表示分子內所含原子的種類、數目及特定的官能基,而顯示其特性的化學式,一般多用於有機化合物。 B、
有機化合物中,代表特定結構的原子或原子團,稱為官能基。常見的官能基: 例如:有機酸含-COOH (羧基);醇類含-OH
(羥基);胺類含-NH2 (胺基)等。 C、 示性式是結構式的簡化。 例:Þ CH (六) 物質的成分分析及測定 A、 有機物的C、H、O元素定量分析──燃燒分析法 B、 測定方法: (1). 將定量的有機試料燃燒產物先通過高溫的CuO(作氧化劑,幫助試料完全氧化)。 (2). 先通過過氯酸鎂Mg(ClO4)2以吸收H2O,再通過氫氧化鈉NaOH以吸收CO2。 (3). 由過氯酸鎂與氫氧化鈉所增加的重量,求得H、C之組成。即:
測得H2O質量求含H的質量=H2O重×
測得CO2質量求含C的質量=CO2重×
若含氧元素,則含O質量=試料質量-C元素質量-H元素質量。 【例1】3 g的某有機化合物完全燃燒以後,得到4.4 g的二氧化碳及1.8
g的水。試求此有機化合物的實驗式及式量為何? 【答案】:簡式為CH2O, 式量=30 【解析】:物質含碳C質量= 物質含氫H質量= 【例2】燃燒維生素C試樣1.76 mg,得二氧化碳2.64 mg和水0.72
mg。 (1) 維生素C的實驗式為何? (2) 若由另一實驗測得其分子量為180,則維生素C分子式及分子量為何? 【答案】:(1)C3H4O3 (2)分子式為C6H8O6;精確的分子量=176 【解析】:物質含碳C質量= 物質含氫H質量= 【例3】在氧氣下燃燒3.42 g只含有氮和氫的化合物,可獲得9.82
g NO2和3.85 g水,若由另一實驗測得此氮氫化合物的分子量為32,則此化合物的分子式為何?(N = 14) 【答案】:N2H4
【解析】:NO2分子量=14+32=46 N佔14/46, 【例4】下列敘述何者正確?(有二答) 【答案】:(A)(E) 【解析】:(A)有相同的分子式,但是結構排列不相同,因此性質不相同,稱為同分異構物。 【例5】下列敘述,何者錯誤? 【答案】:(C) 【解析】:(A)CH3COOH的分子式為C2H4O2,簡式為CH2O,C6H12O6的簡式也是CH2O。 【例6】化合物甲經元素分析得C:54.50%,H:9.18%,其餘為氧;又甲0.33 g汽化後,在200℃及1大氣壓下體積為145 mL;同溫同壓下145 mL的氧氣重0.12 g。求化合物甲之 【答案】:(1)實驗式:C2H4O (2)分子量:88 (3)分子式:C4H8O2 【解析】:假設C有54.5克,H有9.18克,則O質量=100-54.5-9.18=36.32克 【例7】同溫同壓下,某氣體化合物僅含碳、氫、氮三元素,將此化合物與恰能使其完全燃燒所需之氧混合,此混合氣體9體積燃燒後生成4體積的CO2、6體積的水蒸氣及 2體積的氮,則其分子式為何? 【答案】:C2H6N2 【解析】:a
CxHyNz+(9-a)O2 → 4 CO2+6
H2O+2 N2, 【例8】下列何者不為實驗式? 【答案】:(D) 【解析】:(A)KCl為離子化合物,以簡式表示; (B) SiO2為網狀固體,以簡式表示。 【例9】某有機化合物由C、H、N元素組成,高溫下取其氣體 【答案】:(C) 【解析】:假設化合物的化學式為CxHyNz,則
CxHyNz+O2 → x CO2+ 【例10】等重的甲醛(HCHO)、乙酸(CH 【答案】:(A)(C) 【解析】:甲醛(HCHO)、乙酸(CH 【例11】現有某一含C、H、O的液態未知物,將此未知物7.40毫克置於純氧中使其完全燃燒後,產物先通過含無水過氯酸鎂之吸收管,再經氫氧化鈉吸收管,結果過氯酸鎂吸收管重量增加5.40毫克,氫氧化鈉吸收管重量增加13.2毫克,則此未知物的實驗式為何? 【答案】:(C) 【解析】:含C的重量=13.2
´ 【例12】以下哪些物質的化學式可以顯現該物質的特性? 【答案】:(C)(D) 【解析】:示性式能顯示化學物質的部分特性,選項中僅(C)(D)為示性式。 【例13】下列關於葡萄糖和冰醋酸(CH 【答案】:(D)(E) 【解析】:(D)葡萄糖(C6H12O6)與冰醋酸(CH3COOH),有不同的分子式,但是簡式相同,兩者不是同分異構物。 |