|
( )1.
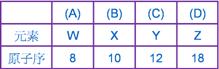
原子序32元素與下列何者化學性質最相似?
【答案】:(B) 【解析】:鈍氣組態為8A族元素,原子序為2,10,18,36,54,86。 ( )2.
下列各數字代表週期表元素之原子序,何組不是同族元素?
【答案】:(A) 【解析】:21∼30為過渡元素,因此(A)12(鎂)、20(鈣)、28(鎳)。 ( )3.
週期表第一至第六週期之元素數目依次為何?
【答案】:(A) 【解析】:鈍氣組態為8A族元素,原子序為2,10,18,36,54,86。 ( )4.
關於週期表第一至第三週期的元素,何者錯誤?
【答案】:(A) 【解析】:硼有3個價電子。共有5個電子,電子組態為(2,3)。 ( )5.
有關元素週期表,下列何項敘述錯誤? 【答案】:(B) 【解析】:(A)鈍氣組態為8A族元素,原子序為2,10,18,36,54,86。 ( )6.
原子序53和 【答案】:(B) 【解析】:53為7A族,-1價元素,為碘I;38為2A族,+2價元素,為鍶Sr; ( )7.
下列各組,何者為週期表之過渡元素? 【答案】:(B) 【解析】: (B)Cu,Ag,Au 皆為B族過渡元素。 ( )8.
下列有關週期表及電子排列的敘述,何者正確? 【答案】:(D) 【解析】:同週期的元素隨著原子序增加,價電子數增加,非金屬性質增強,金屬性質減弱,個元素的化學性質不同。 (B)現在的週期表示依原子序(質子數)排列,不是依照原子量排列。 ( )9.
列哪一元素的價電子數不是7個?
【答案】:(B) 【解析】:氬(Ar)不是鹵素,價電子數有8個。 ( )10.
第三列元素的原子有電子填到第幾層? 【答案】:(C) 【解析】:第3列的元素,週期內的價電子殼層填到M層(n=3)。 |
|
( )11.
下列有關第一列過渡元素的敘述,何者正確?
【答案】:(C) 【解析】:第一列的過度元素為21∼30,共10個元素,全是金屬元素,常溫下皆為固體,僅同週期不同族的元素,價電子數不相同。 ( )12.
矽晶( 【答案】:(C) 【解析】:矽為4A(第14族)元素,矽的氧化物為網狀固體,原子序14,電子組態為(2,8,4),有4個價電子。 ( )13.
有關價電子與化學性質的敘述,何者正確? 【答案】:(C) 【解析】:8A族只有氦He為2個價電子,其餘的元素價電子皆為8個,為價殼層全滿的狀態,性質最安定。 (B)H為+1價的1A族元素,但是不是鹼金族。 (C)硼矽鍺砷銻碲等元素為類金屬元素,導電性介於金屬與非金屬間,為重要的半導體材料。 (D)同週期元素,價電子數愈多,失去電子的能力愈弱,得到電子的能力愈強,因此金屬性質愈弱,非金屬性質愈強,容易形成共價鍵的分子化合物,部分元素能形成網狀固體。 ( )14.
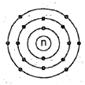
【答案】:(C) 【解析】:右圖的電子組態為(2,8,6),原子序為16,為6A族(第16族)的硫元素。 ( )15.
近年來IUPAC建議廢除族的區別,將元素分為1∼18族,下列元素括號內數字表所屬族數,何者不正確?
【答案】:(B) 【解析】:Al為+3價的元素,為硼族(第13族)元素。 ( )16.
有關週期表中同一族的元素,下列敘述何項完全正確?
【答案】:(C) 【解析】:同一族的元素價電子數目相同,1A的元素都有一個價電子;3A的元素都有3個價電子。 ( )17.
下列說法中,何者錯誤? 【答案】:(C) 【解析】:
(C)原子的最外層的價電子數,等於該元素所在的主族數,即3A有3個價電子,5A有5個價電子。 ( )18.
有關原子中的電子排列及週期表,下列敘述何者正確? 【答案】:(E) 【解析】:(A)門得列夫依"原子量"排列週期表,並預測了一些尚未發現的元素存在。 ( )19.
關於週期表的敘述,何者錯誤? 【答案】:(D) 【解析】:
(D)硫(S)是第三週期第16族元素,電子組態為(2,8,6)因此是6A族元素(或是第16族)。 ( )20.
對原子序12之元素M,正確敘述為 【答案】:(D) 【解析】:原子序12為(2,8,2)是週期表第三週期,2A族(第二族)元素,鹼土族金屬,為+2價元素,因此氫化物為MH2。 |
|
( )21.
下列哪一種元素是金屬? 【答案】:(C) 【解析】:(A)原子序8為(2,6)是6A族元素,非金屬。 (B)原子序10為(2,8)是8A族元素,非金屬氣體。 (C)原子序12為(2,8,2)是2A族元素,金屬。 (B)原子序18為(2,8,8)是8A族元素,非金屬氣體。 ( )22.
門得列夫提出之週期律,因下列何項發現而被修正?
【答案】:(B) 【解析】:門得列夫提出之週期律,是根據原子量排列,實際上在1913年時,英國莫斯利提出以原子序為原子週期排列的根據,獲得一致的接受,成為現今的週期表元素。 ( )23.
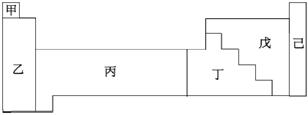
【答案】:(C) 【解析】:半導體元素分布在丁與戊的區域間,為階梯狀排列的元素。 ( )24.
現代週期表的使用,在化學知識的學習提供很大的方便。關於週期表的敘述,何者錯誤? 【答案】:(D) 【解析】:
(D)硫(S)是6A族元素,是第三週期第16族元素,為負二價非金屬。 ( )25.
關於第三列元素,何者錯誤? 【答案】:(D) 【解析】:(B)矽、二氧化矽、鑽石為網狀固體。 ( )26.
下列哪一組元素符號依序為[硼、鈦、鉻、砷、氪]?
【答案】:(D) 【解析】:[硼(B)、鈦(Ti)、鉻(Cr)、砷(As)、氪(Kr)]。 ( )27.
下列哪位化學家依原子量由小而大排列成週期表,並在表中留出若干空位置,預言這些空位置是一些尚未發現的元素,且預言這些尚未發現元素的性質? 【答案】:(C) 【解析】:門得列夫在1896年時,依據原子量由小而大排列成週期表,並預言尚未發現的元素。 ( )28.
關於第三週期元素,何者錯誤? 【答案】:(D) 【解析】:(B)矽、二氧化矽、鑽石為網狀固體。 |